Stellungnahme des AK NEM bezüglich BfR-Empfehlungen zu Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln
- Der Arbeitskreis Nahrungsergänzungsmittel (AK NEM) im BLL nimmt in einer ersten, noch nicht abschließenden Kommentierung Stellung zu den aktuellen Ausführungen und Vorschlägen des BfR zu Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln.
Das Bundesinstitut für Risikobewertung (BfR) hat seine Empfehlungen für Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln aus dem Jahr 2004 (1, 2) auf Basis neuer wissenschaftlicher Erkenntnisse überarbeitet. Die aktualisierten Höchstmengenvorschläge sind im Januar 2018 veröffentlicht worden (3). Wie das BfR ausführt, ist dies vor dem Hintergrund geschehen, dass auf europäischer Ebene noch keine verbindlichen Höchstmengen festgelegt worden sind. Die nun vorliegenden Vorschläge sollen als Entscheidungshilfe für das Risikomanagement des Bundesministeriums für Ernährung und Landwirtschaft (BMEL) dienen und Grundlage für eine gesetzliche Regelung mit nationalen Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln werden.
Die Hersteller von Nahrungsergänzungsmitteln setzen sich seit Jahren für gesetzlich festgelegte Höchstmengen für Vitamine und Mineralstoffe ein, damit Verbraucher und Hersteller in der gesamten Europäischen Union (EU) (Rechts-)Sicherheit haben. Daher wird die Wiederaufnahme der Diskussion um Höchstmengen durch die überfällige Aktualisierung der BfR-Höchstmengenempfehlungen grundsätzlich begrüßt. Zugleich ist festzuhalten, dass es eines offenen europaweiten Diskurses über die zum Teil erheblich unterschiedlichen Interpretationen der wissenschaftlichen Daten und methodischen Ansätze zur Ableitung von Höchstmengen bedarf, weil nur eine europaweit einheitliche Festlegung von Höchstmengen zielführend ist. Unterschiedliche Höchstmengen in verschiedenen Mitgliedstaaten der EU sind in Zeiten, in denen Konsumenten auch über Grenzen hinweg einkaufen, weder zeitgemäß noch zum Verbraucherschutz sinnvoll und stehen im Widerspruch zum Grundsatz des freien Warenverkehrs in der EU.
Vor diesem Hintergrund nimmt der Arbeitskreis Nahrungsergänzungsmittel des BLL in einer ersten, noch nicht abschließenden Kommentierung zu den aktuellen Ausführungen und Vorschlägen des BfR wie folgt Stellung:
1. Rechtsvorgaben und europäischer Kontext
Bereits vor zehn Jahren war der europäische Gesetzgeber fast schon einmal so weit: Nach ausführlicher Diskussion unterschiedlichster Ansätze stand damals die Verständigung auf konkrete Höchstmengen für den Zusatz von Vitaminen und Mineralstoffen zu Nahrungsergänzungsmitteln unmittelbar bevor. Bedauerlicherweise scheiterte eine Einigung nicht zuletzt an der mangelnden Kompromissbereitschaft der Mitgliedstaaten.
Auseinandersetzung mit anderen Sicherheitsbewertungen notwendig
Seinerzeit war es ein von Wissenschaftlern gemeinsam mit der Wirtschaft entwickeltes Modell, das seitens der Europäischen Kommission und der Mehrheit der Mitgliedstaaten große Akzeptanz fand (4). Dieses Modell von Richardson (5) basiert gemäß den Vorgaben des europäischen Gesetzgebers (Artikel 5 Abs. 2 der RL 2002/46/EG (NEM-RL)) auf den Faktoren der tolerierbaren höchsten Tagesaufnahmemengen, den Aufnahmemengen über die normale Ernährung und den Referenzmengen für die Nährstoffzufuhr. Im Unterschied zum BfR-Modell arbeitet es jedoch mit realen Verzehrdaten und faktenbasierten Sicherheitszuschlägen, weshalb auf theoretische Annahmen und Mutmaßungen verzichtet werden kann.
Bereits im Jahr 2014 wurden auf Basis dieses Modells unter Berücksichtigung aktueller wissenschaftlicher Erkenntnisse die Vorschläge für Höchstmengen von Vitaminen und Mineralstoffen in Nahrungsergänzungsmitteln von Professor Richardson überarbeitet (6). Diese sind veröffentlicht und stehen als Beitrag für eine wissenschaftlich fundierte Diskussion zur Verfügung (7). Eine inhaltliche Auseinandersetzung mit dieser wissenschaftlichen Arbeit zur Ableitung von Höchstmengen ist der Publikation mit den aktuellen Höchstmengenempfehlungen des BfR bedauerlicherweise ebenso wenig wie eine inhaltliche Auseinandersetzung mit aktuellen Sicherheitsbewertungen und Empfehlungen anderer Mitgliedstaaten zu entnehmen.
Vorgaben des EuGH sind zu beachten
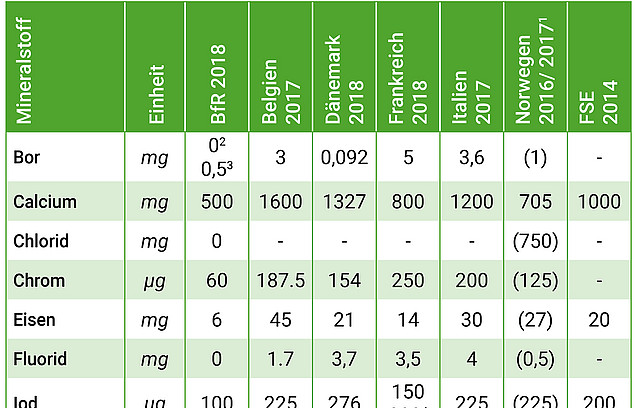
Insbesondere die fehlende Auseinandersetzung mit aktuellen Sicherheitsbewertungen anderer europäischer oder weltweiter Institutionen und Behörden überrascht vor dem Hintergrund der jüngsten EuGH-Entscheidungen. So führt der EuGH in seiner Begründung im Urteil zur französischen Höchstmengenregelung für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln („Noria“, Rs. C-672/15) aus, dass bei der Festsetzung von Höchstmengen die Kriterien des Art. 5 Abs. 1 und 2 der NEM-RL zu berücksichtigen sind, wobei in die Risikobewertung sämtliche zuverlässig vorliegenden Daten, einschließlich der internationalen, einzubeziehen sind. Wie das BfR in seiner Publikation ausführt, hat eine Reihe von Mitgliedstaaten in letzter Zeit Höchstmengen für Vitamine und Mineralstoffe eingeführt bzw. aktualisiert.
Eine Übersicht veranschaulicht die enormen Unterschiede bei den auf nationaler Ebene jeweils als sicher angesehenen Höchstmengen – basierend auf jeweils aktuellen Risikobewertungen. Es ist insbesondere im europäischen Vergleich deutlich erkennbar, dass die Vorschläge des BfR äußerst restriktiv ausfallen. Es stellt sich die Frage, wie die Interpretation gleicher wissenschaftlicher Daten – ohne plausible wissenschaftliche Begründung wegen z. B. stark abweichender Ernährungsgewohnheiten – zu so unterschiedlichen Ergebnissen kommen kann. Dies unterstreicht die Notwendigkeit des wissenschaftlichen und politischen Diskurses auf europäischer Ebene.
Hypothetische Risiken können keine Verbote begründen
Nationale Höchstmengenfestlegungen können nicht grundsätzlich verhindern, dass Produkte, die in anderen Mitgliedsländern der Europäischen Union beispielsweise mit höheren Dosierungen rechtmäßig vermarktet werden, weiterhin auch in Deutschland angeboten werden dürfen. Dem steht das Prinzip der gegenseitigen Anerkennung entgegen. Wie der EuGH sowohl im Noria-Urteil als auch im Queisser-Urteil (Rs. C-282/15) ausführt, darf eine Ablehnung eines (höher dosierten) Produkts nur bei einem tatsächlichen Risiko erfolgen. Dabei reichen rein hypothetische Annahmen von Risiken nicht für ein Verbot aus. Die Tatsache, dass Produkte, die die Mengenempfehlungen einhalten, nach Aussage des BfR auf Basis der vorliegenden Risikobewertung „für Personen ab 15 Jahren sicher“ sind, führt deshalb nicht im Umkehrschluss dazu, dass jedes höher dosierte Produkt als unsicher einzustufen ist.
2. Sicherheitszuschläge und Multiexpositionsfaktoren
Grund für die zum Teil erheblichen Abweichungen zwischen den BfR-Höchstmengenempfehlungen und anderen nationalen Höchstmengenfestlegungen ist der sehr konservative Ansatz des BfR-Modells, das gleich mehrere Sicherheitsstufen beinhaltet.
So hat das BfR seine Höchstmengenempfehlungen nicht nur auf Basis neuer wissenschaftlicher Erkenntnisse überarbeitet, sondern dabei ohne weitere Begründung auch die Zielgruppe verändert. Die Ableitung der Höchstmengen erfolgt nun nicht mehr für Erwachsene, sondern wurde auf Jugendliche der Altersgruppe 15 bis 19-Jährige erweitert. Dies führt dazu, dass in der Ableitung von Höchstmengenempfehlungen die geringeren tolerierbaren Tagesdosen (UL) für Jugendliche (soweit vorhanden) zum Ansatz kommen.
Trennung von Höchstmengenableitung für Jugendliche und Erwachsene notwendig
Diese Vorgehensweise ist schwer nachvollziehbar. Eine Vermischung der Ableitung von Höchstmengen für gesunde Erwachsene und für die sensiblere Bevölkerungsgruppe der Heranwachsenden ist nicht sinnvoll. Wenn eine begründete Notwendigkeit bestehen sollte, für diese Bevölkerungsgruppe eigene Höchstmengen festzusetzen, dann müsste dies in einem gesonderten, zweiten Schritt erfolgen. Verbraucherbefragungen haben im Übrigen ergeben, dass der klassische Konsument von Nahrungsergänzungsmitteln 50 Jahre und älter ist. Bei einer repräsentativen Befragung von deutschen Verbrauchern waren weniger als 2,5 Prozent der Verwender von Nahrungsergänzungsmitteln der Altersklasse 18 bis 24 Jahren zuzuordnen (8).
Des Weiteren arbeitet das BfR auf zwei weiteren Stufen mit pauschalen Sicherheitsfaktoren, die nicht auf wissenschaftlichen Daten oder realen Verzehrs- oder Marktdaten beruhen, sondern sich lediglich auf theoretische Annahmen stützen.
Dabei ist zu beachten, dass bereits durch die Nutzung der beiden Kenngrößen „UL“ und „Aufnahmemenge der deutschen Bevölkerungsgruppe mit der höchsten Nährstoffaufnahme“ ein zweifacher Sicherheitsaufschlag erfolgt. Beim UL handelt es sich laut Definition um eine sichere Zufuhrmenge, die auf eine chronische (tägliche, lebenslange) Aufnahme bezogen ist und zudem selbst bereits Sicherheitsmargen enthält. Die Verwendung der Aufnahmemengen der deutschen Bevölkerungsgruppe mit der höchsten Nährstoffaufnahme (95. Perzentile) durch die normale Ernährung stellt einen weiteren Sicherheitsfaktor dar, da die meisten Menschen in der Realität eine geringere Aufnahmemenge haben.
Arbeiten mit pauschalen Multiexpositionsfaktoren wissenschaftlich fragwürdig
Nun baut das BfR in seinem Modell zwei weitere Sicherheitsebenen pauschal für alle Nährstoffe ein, indem es
- die Restmenge, die zusätzlich zur üblichen Ernährung aufgenommen werden kann, auf Nahrungsergänzungsmittel und angereicherte Lebensmittel aufteilt und
- einen Unsicherheitsfaktor von 2 für eine mögliche Mehrfachexposition eines Nährstoffes durch die Einnahme unterschiedlicher Nahrungsergänzungsmittel einbaut.
Das BfR führt somit bei vielen Nährstoffen den Faktor von 4 für eine theoretische Multiexposition ein; denn die Restmenge als Differenz von UL und der Zufuhr durch traditionelle Lebensmittel wird im Modell letztendlich durch 4 geteilt. Das BfR zieht zur Ableitung von sicheren Höchstmengen für die gesunde deutsche Bevölkerung somit eine hypothetische Verbrauchergruppe heran, die täglich über einen langen Zeitraum, d. h. chronisch, zur allgemeinen Ernährung zusätzlich 2 Nahrungsergänzungsmittel und angereicherte Lebensmittel verzehren soll, die allesamt den gleichen zugesetzten Nährstoff enthalten. Es gibt keine Hinweise dafür, dass eine derartige Annahme der Realität entspricht, ganz im Gegenteil. Die Multiexposition als eigenständiger Risikofaktor durch das BfR ist demzufolge mit den Vorgaben des EuGH im Queisser-Urteil (Rs. C-282/15) schwerlich zu vereinbaren. Mit der Heranziehung einer realitätsfernen Annahme lässt sich das Vorliegen eines tatsächlichen (und nicht nur eines hypothetischen) Risikos nicht begründen. Ferner hat der EuGH bereits 2004 einer derart pauschalen Herangehensweise mit seinen Entscheidungen in Sachen Kommission/Deutschland (Rs. C-387/99) und Kommission/Österreich (Rs. C- 150/00) eine Absage erteilt.
Pauschale Herangehensweise nicht durch reale Verzehr- und Marktdaten gedeckt
So gibt es keine Erhebung, die die Annahme stützt, dass Verbraucher im großen Umfang und vor allem regelmäßig Nahrungsergänzungsmittel und angereicherte Lebensmittel parallel verzehren. Verzehrdaten über die Nährstoffzufuhr von Vitaminen und Mineralstoffen durch angereicherte Lebensmittel in Deutschland sind nicht verfügbar. Jedoch zeigen Marktanalysen, dass angereicherte Lebensmittel insgesamt einen nur kleinen Teil (2016: 4,4 Prozent) der verpackten Lebensmittel in Deutschland ausmachen und entgegen der öffentlichen Wahrnehmung nicht für einen stark wachsenden und dynamischen Markt stehen. Im Gegenteil, der Markt der angereicherten Lebensmittel verzeichnet insgesamt – trotz gemessen am Umsatz leicht positiver Entwicklung – im Zeitraum der letzten Marktanalyse (2011 bis 2016) keinerlei Mengenwachstum. Der Marktanteil von verpackten Lebensmitteln, die mit Vitaminen angereichert waren, lag 2016 bei rund 2,5 Prozent auf ebenfalls konstant niedrigem Niveau mit leicht rückläufiger Tendenz. Die Tatsache, dass der Anteil angereicherter Lebensmittel an der Vitamin- und Mineralstoffzufuhr regelmäßig überschätzt wird, ist nicht neu (9), insbesondere auch deswegen, da ein Großteil der Lebensmittel (unverpackt und unverarbeitet) der Anreicherung überhaupt nicht zugänglich ist.
Repräsentative Daten über die Verwendung von Nahrungsergänzungsmitteln in Deutschland rechtfertigen zudem nicht einen pauschalen Multiexpositionsfaktor von 2 für die theoretische Mehrfachzufuhr eines Nährstoffes durch verschiedene Nahrungsergänzungsmittel. Jüngste Untersuchungen (10) bestätigen die Ergebnisse früherer Untersuchungen (11), wonach nur ein geringer Bevölkerungsanteil täglich mehrere Nahrungsergänzungsmittel verzehrt, die die gleichen Nährstoffe enthalten. Die Verbraucher gehen zumeist verantwortungsbewusst mit Nahrungsergänzungsmitteln um. Sie beachten die Hinweise auf der Verpackung und sind sich der möglichen Risiken einer überhöhten Zufuhr von Nährstoffen bewusst (8). Der verantwortungsvolle Umgang zeigt sich insbesondere darin, dass die Verbraucher bewusst kombinieren, wenn überhaupt mehrere Produkte gleichzeitig konsumiert werden (10). Eine „Multiexposition“, d. h. eine Aufnahme eines Nährstoffes über mehrere Nahrungsergänzungsmittel gleichzeitig, war von geringer Relevanz. Bei 93,8 Prozent der Verwender von Nahrungsergänzungsmittel stammen die jeweiligen Nährstoffe aus einem einzigen Produkt. Es liegen also Daten für die Mehrfacheinnahme von NEM mit gleichen Nährstoffen vor, weshalb die Verwendung eines pauschalen „Unsicherheitsfaktors bezüglich einer unbekannten, aber möglichen Mehrfacheinnahme von NEM mit gleichen Nährstoffen“, nicht zu begründen ist. Die genannten Publikationen werden vom BfR an anderer Stelle erwähnt, es fehlt jedoch eine Auseinandersetzung mit diesen Ergebnissen.
Grundlage einer Risikobewertung müssen reale Verzehrmuster sein
Grundlage einer Risikobewertung müssen reale Verzehrmuster sein, nicht Annahmen oder Mutmaßungen. Die Feststellung der Zufuhr von Vitaminen und Nährstoffen in der Risikobewertung muss daher auf repräsentativen Verzehrerhebungen beruhen. Wenn überhaupt ein Multiexpositionsfaktor zur Anwendung kommen soll, dann ist dieser je Nährstoff differenziert zu betrachten und zu begründen.
3. Modellrechnung und Einzelfallbetrachtung
Das BfR hat in seiner aktuellen Veröffentlichung die Kritik im Hinblick auf die häufige Verwerfung des eigenen Modells, die gegenüber den Ableitungen von Höchstmengen-empfehlungen des BfR aus dem Jahr 2004 geäußert wurde, teilweise berücksichtigt. Insbesondere ist der Verzicht auf eine Mengenbegrenzung für Nährstoffe (Vitamin B1, Vitamin B2, Biotin und Pantothensäure) zu begrüßen, für die aufgrund fehlender Hinweise auf nachteilige Effekte keine UL abgeleitet wurden.
Daten anderer anerkannter Institutionen sind zu berücksichtigen
Es wird jedoch nicht ersichtlich, warum bei fehlender UL-Festsetzung seitens SCF/EFSA nicht konsequent die tolerierbaren Tageshöchstdosen anderer anerkannter Institutionen (IOM, EVM) herangezogen wurden, soweit entsprechende Daten vorliegen. Dies wurde nur im Fall von Eisen so gehandhabt. Insbesondere fehlt die Begründung für die Nichtverwendung dieser UL bei den Nährstoffen, auf die ansonsten das Ableitungsverfahren Anwendung fand (Vitamin C, Kalium oder Chrom). Die fehlende Erläuterung der Gründe für die Nichtberücksichtigung dieser Werte in der Publikation ist bedauerlich, vor allem vor dem Hintergrund der wiederholt formulierten Vorgabe (NEM-RL, Orientierungspapier der Europäischen Kommission 2007, EuGH-Urteil Noria), dass die Risikobewertung auf allgemein anerkannte Daten zu stützen sei und somit notwendigerweise auch Erkenntnisse anderer wissenschaftlicher Gremien zu berücksichtigen sind.
Grundsätzlich ist anzumerken, dass ein wissenschaftlicher Diskurs immer dann notwendig wird, wenn verschiedene anerkannte Gremien wie im Beispiel von Vitamin B6, Vitamin E, Kalium oder Mangan zu stark voneinander abweichenden UL-Ableitungen gelangen. Schließlich dient der UL als Ausgangspunkt für jede Risikobewertung. In Europa ist die EFSA die Institution, die um eine wissenschaftliche (Neu-)Bewertung von UL zu bitten bzw. mit dieser zu beauftragen wäre.
4. Nutzenerwägung und Risikobewertung
Das BfR führt aus, dass bei der Risikobewertung nicht nur Risiken durch eine übermäßige, sondern auch durch eine unzureichende Zufuhr zu berücksichtigen sind. Grundsätzlich ist eine Risiko-Nutzen-Abwägung in der regulatorischen Festsetzung von Höchstmengen zu begrüßen, insbesondere vor dem Hintergrund, dass trotz einer ausreichenden Versorgung auf Bevölkerungsebene die Versorgungslage einzelner Bevölkerungsgruppen oder des Einzelnen unzureichend sein kann. So belegen die Daten der NVSII, dass bei fast allen ausgewerteten Nährstoffen ein Teil der Bevölkerung von einer zusätzlichen Zufuhr durch Supplemente profitieren kann. Bei Verwendern von Nahrungsergänzungsmitteln sinkt der Anteil der Personen, der die Referenzwerte nicht erreicht, bei Vitamin D, E, C, Folsäure, Calcium und Magnesium um 6 bis 25 Prozent.
Trennung von Nutzen- und Risikobewertung notwendig
Eine Vermischung von Nutzenerwägung und Risikobetrachtung im Rahmen einer Sicherheitsbewertung ist jedoch wissenschaftlich und rechtlich fraglich und faktisch nicht zielführend. Eine Bewertung des gesundheitlichen Risikos durch eine zusätzliche Zufuhr und die Diskussion über den Nutzen dieser sind getrennt voneinander zu führen. Nicht gesehene positive gesundheitliche Effekte sind ebenso wie eine auf Bevölkerungsebene ausreichende Versorgung keine Begründung für Restriktionen. Die Festlegung von Höchstmengen in Nahrungsergänzungsmitteln ist mit dem Schutz des Verbrauchers vor nachteiligen Wirkungen für die Gesundheit begründet (Erwägungsgrund 13 der Richtlinie 2002/46/EG) – nicht aber mit dem Bedarf. So entspricht es auch der Rechtsprechung des EuGH (Urteil v. 23.9.2001, C-192/01, Kommission/Dänemark), dass das Fehlen eines Ernährungsbedürfnisses allein nicht ein Verbot des Inverkehrbringens von in den anderen Mitgliedstaaten rechtmäßig hergestellten und/oder in den Verkehr gebrachten Erzeugnissen begründen kann.
Das BfR begründet gleichwohl einige Höchstmengenempfehlungen damit, dass die Datenlage zur Sicherheitsbewertung nicht eindeutig sei, aber für eine Aufnahme oberhalb des Bedarfs keine positiven gesundheitlichen Effekte (Bsp. Vitamin E) gesehen werden oder dass keine Gründe für eine zusätzliche Zufuhr erkennbar sind (Bsp. Phosphor). Es ist fraglich, ob diese Herangehensweise dem Anspruch an eine wissenschaftlich basierte Risikobewertung gerecht wird. Zumal für einige dieser Nährstoffe von EFSA und/oder IOM tolerierbare Tageshöchstmengen (UL) festgesetzt wurden und auf dieser Basis die Ableitung von Höchstmengen möglich gewesen wäre.
Risiken von kranken Bevölkerungsgruppen sind gesondert zu betrachten
In diesem Zusammenhang ist auch noch einmal hervorzuheben, dass Nahrungsergänzungsmittel für die gesunde Allgemeinbevölkerung bestimmt sind. Daher ist es nicht sinnvoll, bei der Ableitung von Höchstmengen z. B. Personen mit chronischen Krankheiten oder Stoffwechselanomalien zu berücksichtigen. Grundsätzlich ist davon auszugehen, dass diese Menschen im Rahmen ihres Krankheitsmanagements besonders geschult wurden und daher über mögliche Wechselwirkungen mit Lebensmitteln und einzelnen Inhaltstoffe aufgeklärt sind. Wenn überhaupt, ist bei Bedarf bei besonderem Schutzbedürfnis einzelner Personengruppen im Rahmen des Risikomanagements über (Warn-)Hinweise auf den Produkten nachzudenken.
5. Zusätzlicher Aspekt: Grundsatz der Verhältnismäßigkeit
Bereits im ersten Diskussionsvorschlag aus 2006 (12) verweist die Europäische Kommission darauf, dass mit Blick auf die Art und Weise der Gewährleistung der Sicherheit die primärrechtlichen Vorgaben – so auch der Grundsatz der Verhältnismäßigkeit – zu befolgen sind. Dieser Grundsatz ist umso mehr auf nationaler Ebene zu berücksichtigen, führt doch eine zu restriktive Herangehensweise, die nicht mit einem Sicherheitsrisiko der Verbraucher begründet ist, zu einer unnötigen Benachteiligung der inländischen Unternehmen der Nahrungsergänzungsmittelbranche. Würden die Höchstmengenvorschläge des BfR in der vorgeschlagenen Form umgesetzt werden, würden die deutschen Unternehmen im Binnen- und Exportgeschäft mit starken Umsatzrückgängen rechnen müssen.
Keine unnötige Benachteiligung inländischer Unternehmen
Erstens drohte eine Verschiebung der Nachfrage hin zu höher dosierten Produkten, die ausländische Anbieter unter Berufung auf den Grundsatz der gegenseitigen Anerkennung weiterhin in Deutschland vermarkten dürfen. Darüber hinaus ist zu befürchten, dass die Verbraucher vermehrt Produkte aus dem Internet beziehen, sollten sie „ihre“ Produkte nicht mehr im Markt finden. Dies ist aus Sicht des Verbraucherschutzes sicher nicht wünschenswert. Neben den seriösen Online-Angeboten werden bekanntlich gerade im Internet oftmals Produkte vertrieben, die bereits heute illegal in Hinsicht auf Bewerbung, Zusammensetzung und Dosierung sind.
Zweitens drohten deutschen Unternehmen große Einbußen im Export, denn für die Warenausfuhr werden in einigen Drittländern u. a. spezielle Bescheinigungen über die Verkehrsfähigkeit des Produktes in Deutschland benötigt, die sogenannten Verkehrsfähigkeits- bzw. Exportbescheinigungen (free-sale-certificates). Viele Drittländer erlauben die Vermarktung von Produkten, die bereits für den europäischen Markt zugelassen sind. Hierzu müssen Hersteller nachweisen können, dass ihre Produkte dort tatsächlich legal vermarket werden dürfen. Diesen Nachweis bekommen sie z. B. in Deutschland in Form einer Bestätigung durch die zuständigen Behörden. Es besteht zu befürchten, dass diese nur noch free-sale-certificates für Produkte mit den entsprechend niedrigen Vitamin- und Mineralstoffmengen ausstellen werden, deutsche Unternehmen aber mit niedrig dosierten Produkten in vielen Exportmärkten nicht mehr wettbewerbsfähig wären.
6. Fazit
Die Festsetzung von Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln, wie vom europäischen Gesetzgeber vorgesehen, ist nicht nur aus Sicht des Verbraucherschutzes zu begrüßen, dient sie doch zugleich der (Rechts-)Sicherheit für Unternehmen und garantiert den freien Warenverkehr in Europa. Diese Ziele können jedoch nur erreicht werden, wenn Höchstmengen wissenschaftlich fundiert, europaweit implementiert und dabei verhältnismäßig sind.
- Dem werden die aktuellen Empfehlungen des BfR aus den vorab skizzierten Gründen nur unzureichend gerecht. Zusammengefasst gründet die Kritik vor allem auf folgenden Punkten:
- Eine Risikobewertung muss ausschließlich wissenschaftlich begründet und faktenbasiert erfolgen. Dies beinhaltet, dass mit realen Verzehrdaten und faktenbasierten Sicherheitszuschlägen gearbeitet werden muss. Die Arbeit mit pauschalen, wissenschaftlich unbegründeten Sicherheitsfaktoren widerspricht diesem Ansatz.
- Die Ableitung von Höchstmengen für Vitamine und Mineralstoffe für Erwachsene einerseits und Jugendliche sowie gegebenenfalls anderer Risikogruppen anderseits sollte getrennt voneinander erfolgen.
- Nach der Rechtsprechung sind in die Risikobewertung alle relevanten Erkenntnisse einzubeziehen. Dies schließt auch die wissenschaftliche Auseinandersetzung mit bereits existierenden Empfehlungen, insbesondere der von anderen europäischen oder weltweiten Institutionen und Behörden ein. Der europäische Vergleich zeigt, dass die BfR-Vorschläge unverhältnismäßig restriktiv sind.
- Die Sicherheit steht im Vordergrund der Ableitung von Höchstmengen. Ein zu restriktiver Ansatz, der nicht dem Gesundheitsschutz der gesunden, erwachsenen Bevölkerung geschuldet ist, ist unverhältnismäßig. Es schränkt die Produktauswahl für den Verbraucher unnötig ein und benachteiligt die inländische Lebensmittelwirtschaft im Inland und im Export.
- Der wissenschaftliche und politische Diskurs muss europaweit geführt werden, denn eine europaweit einheitliche Festlegung von Höchstmengen für Vitamine und Mineralstoffe ist unerlässlich. Unterschiedliche Höchstmengen in verschiedenen Mitgliedstaaten der EU sind in Zeiten, in denen Konsumenten auch über Grenzen hinweg einkaufen, weder zeitgemäß noch zum Verbraucherschutz sinnvoll.
Quellen
- BfR 2004a. Verwendung von Vitaminen in Lebensmitteln. Herausgegeben von Domke A, Großklaus R, Niemann B, Przyrembel H, Richter K, Schmidt E, Weißenborn A, Wörner B, Ziegenhagen R. BfR Wissenschaft 03/2004
- BfR 2004b. Verwendung von Mineralstoffen in Lebensmitteln. Herausgegeben von Domke A, Großklaus R, Niemann B, Przyrembel H, Richter K, Schmidt E, Weißenborn A, Wörner B, Ziegenhagen R. BfR Wissenschaft 04/2004
- Weißenborn et al. 2018. Höchstmengen für Vitamine und Mineralstoffe in Nahrungsergänzungsmitteln. J Consum Prot Food Saf; doi.org/10.1007/s00003-017-1140-y
- European Commission 2007. Orientation paper on setting maximum and minimum amounts for vitamins and minerals in foodstuffs. SANCO/E4/ FDA/bs D/540510, Brussels, Belgium
- Richardson 2007. Risk management of vitamins and minerals: a risk categorisation model for the setting of maximum levels in food supplements and fortified foods. Food Science and Technology Bulletin: Functional Foods 4 (6): 51–66.
- Richardson 2014. Risk management approaches to the setting of maximum levels of vitamins and minerals in food supplements for adults and for children aged 4–10 years. http://www.foodsupplementseurope.org/publications-guidelines/.
- Richardson 2015. School of Chemistry, Food and Pharmacy, University of Reading, UK. Risk analysis approaches for establishing maximum levels of essential nutrients in fortified foods and food (dietary supplements). In Science and the Law: How the communication of science affects policy development in the environment, food, health and transport section. Chapter 9, pp 153–173. Chapter DOI 10.1021/bk-2015-1207.ch 009. ACS Symposium Series, Vol. 1207, ISBN 13: 97808411231085. Copyright @ 2015 American Chemical Society
- Heinemann et al. 2015. Verwendung von Nahrungsergänzungsmitteln mit Vitami-nen und Mineralstoffen – Ergebnisse einer deutschlandweiten Verbraucherbefra-gung. J Verbr Lebensm; 2: 131–142
- Godfrey et al. 2004: The impact of fortified foods on total dietary consumption in Europe. British Nutrition Foundation Nutrition Bulletin 29: 188-198
- Willers J et al. 2015. Welche Bedeutung besitzt die Mehrfachverwendung von Nahrungsergänzungsmitteln? Daten einer deutschlandweiten Verbraucherbefragung. J Verbr Lebensm; 2: 1–9
- Beitz et al. 2004. Vitamin- und Mineralstoffsupplementierung in Deutschland. Bundesgesundheitsblatt 47: 1057-1065
- European Commission 2006. Discussion Paper on the setting of maximum and minimum amounts for vitamins and minerals in foodstuffs. Brussels, Belgium
Eine englischsprachige Version dieser Stellungnahme steht hier zur Verfügung:
Initial comments on BfR recommendations for maximum levels for vitamins and minerals in food supplements by Food Supplements Working Group at the BLL (AK NEM)
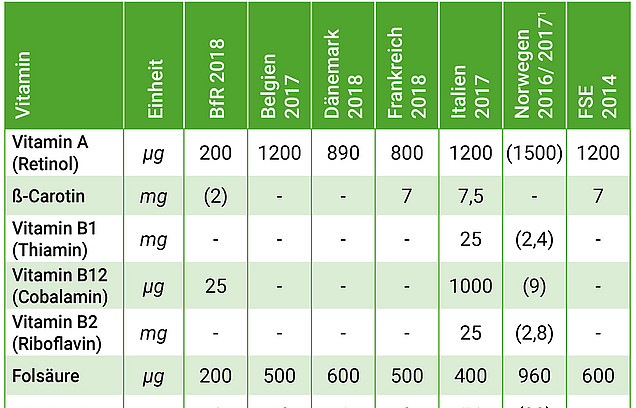
Nationale Höchstmengen(vorschläge) für Vitamine
Infografik anzeigen